净化车间空气洁净度是医药、电子、精密制造等行业核心生产要素,需严格遵循国家/国际技术标准,通过标准化检测流程、精准仪器分析及系统化质量控制,为车间洁净度等级认定、合规验收及持续改进提供技术支撑。商丘净化车间空气洁净度检测的核心依据为“国家标准+行业规范+国际标准”三重体系,不同行业的检测指标与等级要求存在明确技术差异,需精准匹配适用标准。
一、核心技术标准分类与适用范围
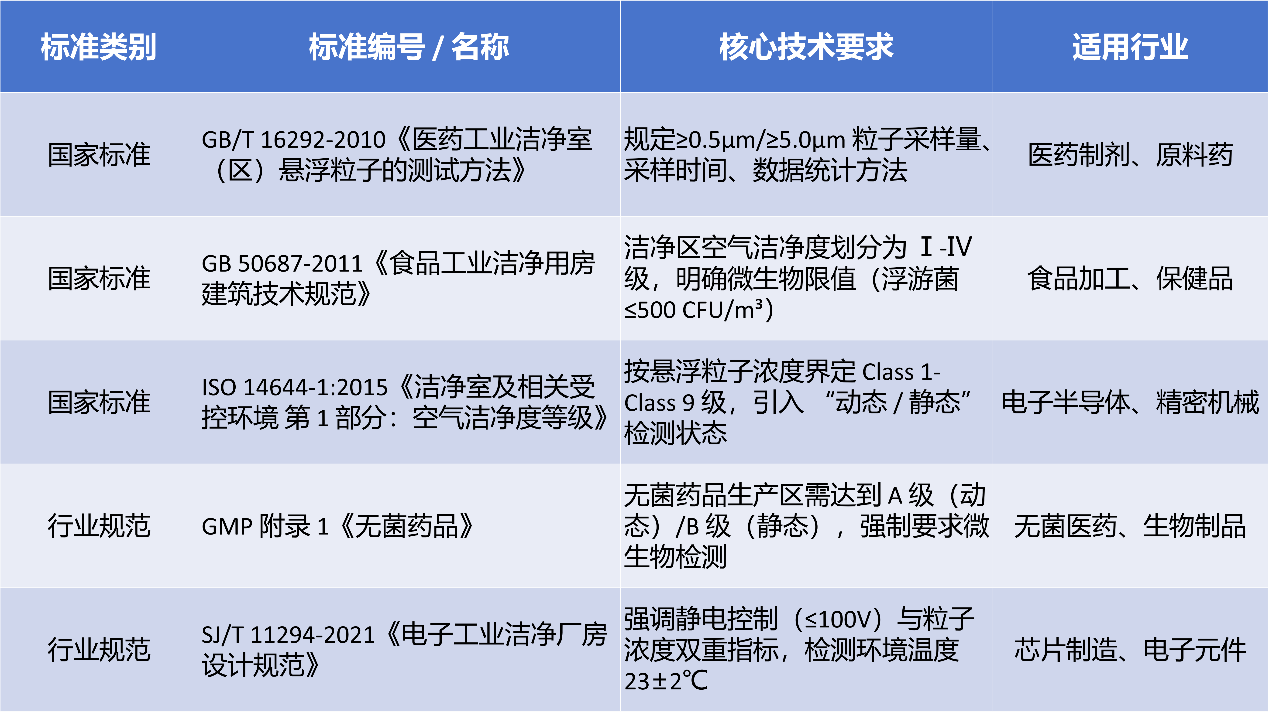
商丘净化车间空气洁净度检测需根据车间功能定位选择对应标准,例如无菌注射剂车间需同时满足GB/T16292与GMP要求,而商丘电子信息产业园的芯片封装车间需执行ISO14644-1Class5级标准。
二、空气洁净度等级核心参数界定
1.悬浮粒子浓度:
ISO14644-1Class5级(静态):≥0.5μm粒子≤3520pc/m³、≥5.0μm粒子≤29pc/m³(适用于商丘芯片封装车间);
GMPA级(动态):≥0.5μm粒子≤3520pc/m³、≥5.0μm粒子≤20pc/m³(严于静态标准,因动态生产中人员/设备会增加粒子污染,适用于商丘无菌注射剂车间)。
2.微生物指标:
GMPB级(静态):浮游菌≤100CFU/m³、沉降菌≤5CFU/4h・φ90mm;
食品GB50687Ⅰ级:浮游菌≤10CFU/m³(适用于商丘婴幼儿配方食品灌装车间)。
3.压差控制:
按GB50457-2019《医药工业洁净厂房设计标准》要求,洁净区与非洁净区压差≥10Pa,不同洁净等级区域压差≥5Pa,气流需从高洁净级向低洁净级单向流动(商丘生物制药车间需额外检测“负压隔离区压差稳定性”,波动≤±2Pa)。

三、检测机构的技术资质认定
1.CMA资质:检测项目需包含“洁净室及相关受控环境检测”,实验室需通过CNAS-CL01:2018《检测和校准实验室能力认可准则》。
2.人员资质:检测工程师需持有“洁净室检测技术培训证书”,微生物检测人员需具备“生物安全培训合格证”。
3.设备要求:实验室需配备符合标准的检测设备,且建立“设备台账-校准记录-使用日志”全生命周期管理体系。

四、检测报告的技术规范
商丘净化车间空气洁净度检测报告需包含以下核心技术内容:
检测依据(明确标准编号及版本,如GB50457-2019);
检测状态(静态/动态,注明人员、设备在场情况);
采样点分布图(标注坐标、面积、采样量);
原始数据记录表(含平行样数据、校准记录);
结果判定(对照标准限值,明确“合格/不合格”);
技术建议(针对不合格项,给出可操作的整改方案);
附件(仪器校准证书复印件、CMA资质证书编号)。
净化车间空气洁净度检测并非单一的合规性检测,而是需融入车间设计、建设、运维全流程的技术管理手段。商丘地区企业应根据行业特性选择符合标准的检测方案,通过定期检测(建议新建车间每季度1次,运维车间每半年1次)及时发现洁净度隐患,同时依托本地具备CMA/CNAS资质的检测机构,获取精准、权威的检测数据,为净化车间的质量控制提供技术保障。
