
一、检测流程(10 步闭环)
1、需求确认
甲方提供:洁净等级(ISO5-ISO8 / A-D级)、面积、关键工艺点、运行模式(静态/动态)。
乙方输出:检测方案(TP)、采样示意图、计划排程。
2、文件审核
设计确认图纸、HVAC 风量平衡表、高效过滤器出厂扫描报告等。
3、预检
开机自净 ≥30 min;确认压差、温湿度、照度已达标。
4、仪器校准
粒子计数器、浮游菌采样器、压差计、风量罩、照度计——全部持有校准证书且在有效期内。
5、采样布点
按“面积平方根法”确定最少点数 N_L = √A(向上取整);高风险区再按 1 点/0.5 m² 加密。

6、现场采样
同步记录:运行状态、人员数、设备转速;自动生成电子原始记录。
7、实验室培养
浮游菌:TSA 培养 48 h(30-35 ℃);
沉降菌:TSA 培养 48 h,再转沙氏琼脂 5 天(真菌)。
8、数据处理
95 % UCL 计算、t-分布(k=1.9),出具 PASS/FAIL 判定。
9、不符合项整改
8D 报告 → 风险评估 → 重新测试(仅对数据超标点位项目)。
10、报告签发
出具的报告需加盖 CMA 资质认定标志及检验检测专用章,电子扫描版报告通过邮件发送至指定邮箱,同时纸质版报告将快递邮寄至预留地址
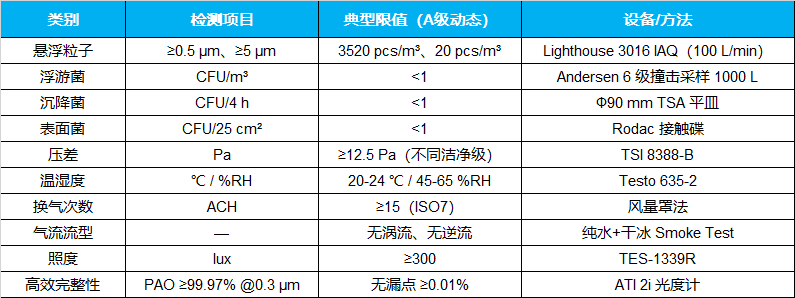
二、检测项目与限值对照表
三、核心依据标准汇总
1、国际标准
ISO 14644-1:2015 洁净室及相关受控环境 第1部分:空气洁净度分级
ISO 14644-3:2019 测试方法(压差、气流、高效检漏)
ISO 14698-1/2:2003 生物污染控制
2、法规与指南
中国《药品生产质量管理规范(2020 修订)》附录1
3、国家标准
GB 50591-2010 洁净室施工及验收规范
GB/T 16292-2010 医药工业洁净室(区)悬浮粒子测试方法
GB/T 16293-2010医药工业洁净室(区)浮游菌的测试方法
GB/T 16294-2010医药工业洁净室(区)沉降菌的测试方法
4、行业规范
EN 1822-4/5 高效过滤器扫描检漏
